Скачать с ютуб Type of Bonds for CH4 (Methane) в хорошем качестве
Скачать бесплатно и смотреть ютуб-видео без блокировок Type of Bonds for CH4 (Methane) в качестве 4к (2к / 1080p)
У нас вы можете посмотреть бесплатно Type of Bonds for CH4 (Methane) или скачать в максимальном доступном качестве, которое было загружено на ютуб. Для скачивания выберите вариант из формы ниже:
Загрузить музыку / рингтон Type of Bonds for CH4 (Methane) в формате MP3:
Если кнопки скачивания не
загрузились
НАЖМИТЕ ЗДЕСЬ или обновите страницу
Если возникают проблемы со скачиванием, пожалуйста напишите в поддержку по адресу внизу
страницы.
Спасибо за использование сервиса savevideohd.ru
Type of Bonds for CH4 (Methane)
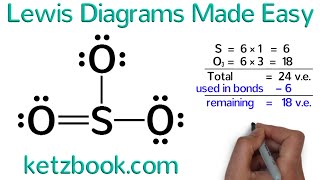
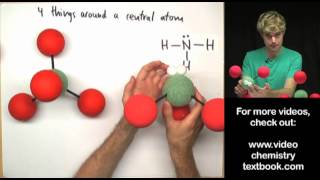
For CH4 (Methane) the type of bonds between atoms are considered covalent (molecular). This occurs when two non-metal atoms bond and electron pairs are shared between atoms. For single bonds one pair of electrons are shared, for double bonds two pairs, and for triple bonds, three pairs are shared. The central Carbon atom Methane has a single bond to each Hydrogen atom. Resources for determining type of bonds: CO2 Lewis Structure: • CO2 Lewis Structure - How to Draw the... Metals & Non-metals: • Metals, Nonmetals, and Metalloids on ... Finding Valence Electrons (element): • Finding the Number of Valence Electro... How to Draw Lewis Structures: • How to Draw Lewis Structures: Five Ea... For CH4 the bonds between the C and O will be slightly due to a small difference in electronegativity values for C and H. However, because the CH4 molecule is tetrahedral and each H atom is on opposite sides, the dipole will cancel and the net dipole for CH4 will be zero. Therefore, the Methane molecule will be non-polar.